Гомологический ряд алкенов. Построение названий алкенов
В органической химии можно встретить углеводородные вещества с разным количеством углерода в цепи и C=C-связью. Они являются гомологами и называются алкенами. Из-за своего строения они химически более активны, чем алканы. Но какие именно реакции для них характерны? Рассмотрим их распространение в природе, разные способы получения и применение.
Что из себя представляют?
Алкены, которые также называются олефинами (маслянистые) получили свое название от этен-хлорида, производного первого представителя этой группы. У всех алкенов есть хотя бы одна двойная C=C-связь. C n H 2n - формула всех олефинов, а название образовывается от алкана с таким же количеством углеродов в молекуле, только суффикс -ан меняется на -ен. Арабской цифрой в конце названия через дефис обозначают номер углерода, от которого начинается двойная связь. Рассмотрим основные алкены, таблица поможет вам запомнить их:
Если молекулы имеют простое неразветвленное строение, то добавляют суффикс -илен, это также отражено в таблице.
Где их можно встретить?
Так как реакционная способность алкенов весьма высока, их представители в природе встречаются крайне редко. Принцип жизни молекулы олефинов — "давай дружить". Нет вокруг других веществ — не беда, будем дружить между собой, образуя полимеры.
Но они есть, и небольшое количество представителей входит в состав сопутствующего нефтяного газа, а высших — в нефти, добываемой на территории Канады.
Самый первый представитель алкенов этен — это гормон, стимулирующий созревание плодов, поэтому его в небольших количествах синтезируют представители флоры. Есть алкен цис-9-трикозен, который у самок мухи домашней играет роль полового аттрактанта. Еще его называют мускалур. (Аттрактант — вещества природного или синтетического происхождения, которое вызывает влечение к источнику запаха у другого организма). С точки зрения химии, алкен этот выглядит так:
Так как весьма ценным сырьем являются все алкены, способы получения их искусственным путем весьма разнообразны. Рассмотрим наиболее распространенные.
А если нужно много?
В промышленности класс алкенов, в основном, получается при крекинге, т.е. расщеплении молекулы под воздействием высоких температур, высших алканов. Для реакции необходим нагрев в диапазоне от 400 до 700 °C. Расщепляется алкан так, как ему захочется, образуя алкены, способы получения которых мы рассматриваем, с большим количеством вариантов строения молекул:
C 7 H 16 -> CH 3 -CH=CH 2 + C 4 H 10.
Еще один распространенный способ называется дегидрирование, при котором от представителя ряда алкана в присутствии катализатора отделяют молекулу водорода.
В лабораторных условиях алкены и способы получения отличаются, они основаны на реакциях элиминирования (отщепления группы атомов без их замещения). Чаще всего элиминируются атомы воды из спиртов, галогены, водород или галогенводород. Наиболее распространенный способ получения алкенов — из спиртов в присутствии кислоты, как катализатора. Возможно использование и других катализаторов
Все реакции элиминирования подчинены правилу Зайцева, гласящему:
Атом водорода отщепляется от того углерода, соседствующего с углеродом, несущим группу -OH, у которого меньше водородов.

Применив правило, ответьте, какой продукт реакции будет преобладать? Позже вы узнаете, правильно ли ответили.
Химические свойства
Алкены активно реагируют с веществами, разрывая свою пи-связь (еще одно название связи C=C). Ведь она не такая прочная, как одинарная (сигма-связь). Углеводород из ненасыщенного превращается в насыщенный, не образуя других веществ после реакции (присоединение).
- присоединение водорода (гидрирование). Присутствие катализатора и нагревания нужна для ее прохождения;
- присоединение молекул галогенов (галогенирование). Является одной из качественных реакций на пи-связь. Ведь при реакции алкенов с бромной водой, она из бурой становится прозрачной;
- реакция с галогенводородами (гидрогалогенирование);
- присоединение воды (гидратация). Условиями прохождения реакции является нагревание и присутствие катализатора (кислоты);
Реакции несимметричных олефинов с галогенводородами и водой подчиняются правилу Марковникова. А значит, водород присоединится к тому углероду из двойной углерод-углеродной связи, у которого уже больше атомов водорода.

- горение;
- неполное окисление каталитическое. Продуктом являются циклические оксиды;
- реакция Вагнера (окисление перманганатом в нейтральной среде). Эта реакция алкенов — еще одна качественная C=C-связь. При протекании розовый раствор марганцовки обесцвечивается. Если ту же реакцию провести в соединенной кислой среде, продукты будут уже другими (карбоновые кислоты, кетоны, углекислый газ);
- изомеризация. Характерны все виды: цис- и транс-, перемещение двойной связи, циклизация, скелетная изомеризация;
- полимеризация — главное свойство олефинов для промышленности.
Применение в медицине
Большое практическое значение имеют продукты реакции алкенов. Многие из них используются в медицине. Из пропена получают глицерин. Этот многоатомный спирт является прекрасным растворителем, причем, если его использовать вместо воды, растворы будут более концентрированными. В медицинских целях в нем растворяют алкалоиды, тимол, йод, бром и др. Также глицерин применяют при приготовлении мазей, паст и кремов. Он предотвращает их высыхание. Сам по себе глицерин является антисептиком.
При реакции с хлороводородом получаются производные, которые применяются как местная анестезия при нанесении на кожу, а также для кратковременного наркоза при незначительных хирургических вмешательствах, при помощи ингаляций.

Алкадиены — это алкены с двумя двойными связями в одной молекуле. Основное их применение — производство синтетического каучука, из которого потом изготавливают различные грелки и спринцовки, зонды и катетеры, перчатки, соски и многое другое, что просто незаменимо при уходе за больными.
Применение в промышленности
| Вид промышленности | Что применяют | Каким образом могут использовать |
| Сельское хозяйство | этен | ускоряет созревание овощей и фруктов, дефолиация растений, пленки для теплиц |
| Лако-красочная | этен, бутен, пропен и др. | для получения растворителей, эфиров, сольвента |
| Машиностроение | 2-метилпропен, этен | производство синтетического каучука, смазочные масла, антифриз |
| Пищевая промышленность | этен | производство тефлона, этилового спирт, уксусная кислота |
| Химическая промышленность | этен, полипропилен | получают спирты, полимеры (поливинилхлорид, полиэтилен, поливинилацетат, полиизобтилен, уксусный альдегид |
| Горная промышленность | этен и др. | взрывчатые вещества |
Более широкое применение нашли алкены и их производные в промышленности. (Где и как используются алкены, таблица выше).

Это лишь малая часть использования алкенов и их производных. С каждым годом потребность в олефинах только возрастает, а значит, возрастает потребность и в их производстве.
ОПРЕДЕЛЕНИЕ
Алкенами называются ненасыщенные углеводороды, молекулы которых содержат одну двойную связь. Строение молекулы алкенов на примере этилена приведено на рис. 1.
Рис. 1. Строение молекулы этилена.
По физическим свойствам алкены мало отличаются от алканов с тем же числом атомов углерода в молекуле. Низшие гомологи С 2 - С 4 при нормальных условиях - газы; С 5 - С 17 - жидкости; высшие гомологи - твердые вещества. Алкены нерастворимы в воде. Хорошо растворимы в органических растворителях.
Получение алкенов
В промышленности алкены получают при переработке нефти: крекингом и дегидрированием алканов. Лабораторные способы получения алкенов мы разделили на две группы:
- Реакции элиминирования (отщепления)
— дегидратация спиртов
CH 3 -CH 2 -OH → CH 2 =CH 2 + H 2 O (H 2 SO 4 (conc) , t 0 = 170).
— дегидрогалогенированиемоногалогеналканов
CH 3 -CH(Br)-CH 2 -CH 3 + NaOH alcohol → CH 3 -CH=CH-CH 3 + NaBr + H 2 O (t 0).
— дегалогенированиедигалогеналканов
CH 3 -CH(Cl)-CH(Cl)-CH 2 -CH 3 + Zn(Mg) → CH 3 -CH=CH-CH 2 -CH 3 + ZnCl 2 (MgCl 2).
- Неполное гидрирование алкинов
CH≡CH + H 2 →CH 2 =CH 2 (Pd, t 0).
Химические свойства алкенов
Алкены - весьма реакционноспособоные органические соединения. Это объясняется их строением. Химия алкенов - это химия двойной связи. Типичные реакции для алкенов - реакции электрофильного присоединения.
Химические превращения алкенов протекают с расщеплением:
1) π-связи С-С (присоединение, полимеризация и окисление)
— гидрирование
CH 3 -CH=CH 2 + H 2 → CH 3 -CH 2 -CH 2 (kat = Pt).
— галогенирование
CH 3 -CH 2 -CH=CH 2 + Br 2 → CH 3 -CH 2 -CH(Br)-CH 2 Br.
— гидрогалогенирование (протекает по правилу Марковникова: атом водорода присоединяется преимущественно к более гидрированному атому углерода)
CH 3 -CH=CH 2 + H-Cl → CH 3 -CH(Cl)-CH 3 .
— гидратация
CH 2 =CH 2 + H-OH → CH 3 -CH 2 -OH (H + , t 0).
— полимеризация
nCH 2 =CH 2 → -[-CH 2 -CH 2 -]- n (kat, t 0).
— окисление
CH 2 =CH 2 + 2KMnO 4 + 2KOH → HO-CH 2 -CH 2 -OH + 2K 2 MnO 4 ;
2CH 2 =CH 2 + O 2 → 2C 2 OH 4 (эпоксид) (kat = Ag,t 0);
2CH 2 =CH 2 + O 2 → 2CH 3 -C(O)H (kat = PdCl 2 , CuCl).
2) σ- и π-связей С-С
CH 3 -CH=CH-CH 2 -CH 3 + 4[O] → CH 3 COOH + CH 3 CH 2 COOH (KMnO 4 , H +, t 0).
3) связей С sp 3 -Н (в аллильном положении)
CH 2 =CH 2 + Cl 2 → CH 2 =CH-Cl + HCl (t 0 =400).
4) Разрыв всех связей
C 2 H 4 + 2O 2 → 2CO 2 + 2H 2 O;
C n H 2n + 3n/2 O 2 → nCO 2 + nH 2 O.
Применение алкенов
Алкены нашли применение в различных отраслях народного хозяйства. Рассмотрим на примере отдельных представителей.
Этилен широко используется в промышленном органическом синтезе для получения разнообразных органических соединений, таких как галогенопроизводные, спирты (этанол, этиленгликоль), уксусный альдегид, уксусная кислота и др. В большом количестве этилен расходуется для производства полимеров.
Пропилен используется как сырье для получения некоторых спиртов (например, пропанола-2, глицерина), ацетона и др. Полимеризацией пропилена получают полипропилен.
Примеры решения задач
ПРИМЕР 1
| Задание | При гидролизе водным раствором гидроксида натрия NaOH дихлорида, полученного присоединением 6,72 л хлора к этиленовому углеводороду, образовалось 22,8 г двухатомного спирта. Какова формула алкена, если известно, что реакции протекают с количественными выходами (без потерь)? |
| Решение | Запишем уравнение хлорирования алкена в общем виде, а также реакцию получения двухатомного спирта:
C n H 2 n + Cl 2 = C n H 2 n Cl 2 (1); C n H 2 n Cl 2 + 2NaOH = C n H 2 n (OH) 2 + 2HCl (2). Рассчитаем количество вещества хлора: n(Cl 2) = V(Cl 2) / V m ; n(Cl 2) = 6,72 / 22,4 = 0,3 моль, следовательно, дихлорида этилена тоже будет 0,3 моль (уравнение 1), двухатомного спирта также должно получиться 0,3 моль, а по условию задачи это 22,8 г. Значит молярная масса его будет равна: M(C n H 2 n (OH) 2) = m(C n H 2 n (OH) 2) / n(C n H 2 n (OH) 2); M(C n H 2 n (OH) 2) = 22,8 / 0,3 = 76 г/моль. Найдем молярную массу алкена: M(C n H 2 n) = 76 - (2×17) = 42 г/моль, что соответствует формуле C 3 H 6 . |
| Ответ | Формула алкенаC 3 H 6 |
ПРИМЕР 2
| Задание | Сколько граммов потребуется для бромирования 16,8 г алкена, если известно, что при каталитическом гидрировании такого же количества алкена присоединилось 6,72 л водорода? Каков состав и возможное строение исходного углеводорода? |
| Решение | Запишем в общем виде уравнения бромирования и гидрирования алкена:
C n H 2 n + Br 2 = C n H 2 n Br 2 (1); C n H 2 n + H 2 = C n H 2 n +2 (2). Рассчитаем количество вещества водорода: n(H 2) = V(H 2) / V m ; n(H 2) = 6,72 / 22,4 = 0,3 моль, следовательно, алкена тоже будет 0,3 моль (уравнение 2), а по условию задачи это 16,8 г. Значит молярная масса его будет равна: M(C n H 2n) = m(C n H 2n) / n(C n H 2n); M(C n H 2 n) = 16,8 / 0,3 = 56 г/моль, что соответствует формуле C 4 H 8 . Согласно уравнению (1) n(C n H 2 n) :n(Br 2) = 1:1, т.е. n(Br 2) = n(C n H 2 n) = 0,3 моль. Найдем массу брома: m(Br 2) = n(Br 2) × M(Br 2); M(Br 2) = 2×Ar(Br) = 2×80 = 160 г/моль; m(MnO 2) = 0,3 × 160 = 48 г. Составим структурные формулы изомеров: бутен-1 (1), бутен-2 (2), 2-метилпропен (3), циклобутан (4). CH 2 =CH-CH 2 -CH 3 (1); CH 3 -CH=CH-CH 3 (2); CH 2 =C(CH 3)-CH 3 (3); |
| Ответ | Масса брома равна 48 г |
Для алкенов характерны, прежде всего, реакции присоединения по двойной связи. В основном эти реакции идут по ионному механизму. Пи-связь разрывается, и образуются две новые сигма-связи. Напомню, что для алканов типичными были реакции замещения и шли они по радикальному механизму. Присоединяться к алкенам могут молекулы водорода, эти реакции называются гидрирование, молекулы воды, гидратация, галогены галогенирование, галогенводороды гидрогалогенирование. Но обо всем по порядку.
Реакции присоединения по двойной связи
Итак, первое химическое свойство способность присоединять галогеноводороды, гидрогалогенирование.
Пропен и остальные алкены реагируют с галогеноводородами по правилу Марковникова.
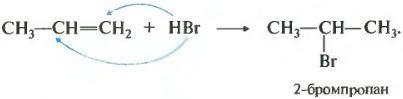
Атом водорода присоединяется к наиболее гидрированному, или правильнее сказать гидрогенизированному, атому углерода.
Вторым номером в нашем списке свойств будет гидратация, присоединение воды.
Реакция проходит при нагревании в присутствии кислоты обычно серной или фосфорной. Присоединение воды происходит также по правилу Марковникова, то есть первичный спирт можно получить только гидратацией этилена, остальные неразветвленные алкены дают вторичные спирты.
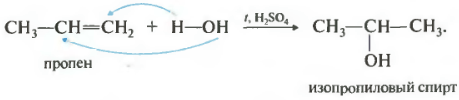
И для гидрогалогениерования и для гидратации существуют исключения из правила Марковникова. Во-первых, против этого правила присоединение протекает в присутствии пероксидов.
Во-вторых, для производных алкенов, в которых присуствуют электронноакцепторне группы. Например, для 3,3,3-трифторпропена-1.

Атомы фтора за счет высокой электроотрицательности оттягивают на себя электронную плотность по цепи сигма-связей. Такое явление называется отрицательным индуктивным эффектом.

Из-за этого происходит смещение подвижных пи-электронов двойной связи и у крайнего атома углерода оказывается частичный положительный заряд, который обычно обозначается как дельта плюс. Именно к нему и пойдет отрицательно заряженный ион брома, а катион водорода присоединится к наименее гидрированному атому углерода.
Помимо трифторметильной группы отрицательным индуктивным эффектом обладает, например, трихлорметильная группа, нитрогруппа, карбоксильная группа и некоторые другие.
Этот второй случай нарушения правила Марковникова в ЕГЭ встречается очень редко, но все-таки желательно иметь его в виду, если вы планируете сдать экзамен на максимальный балл.
Третье химическое свойство присоединение молекул галогенов.
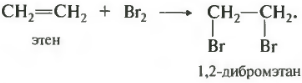
В первую очередь это касается брома, поскольку данная реакция является качественной на кратную связь. При пропускании, например, этилена через бромную воду, то есть раствор брома в воде, имеющий коричневый цвет, происходит ее обесцвечивание. Если пропускать через бромную воду смесь газов, например, этан и этен, то можно получить чистый этан без примеси этена, поскольку тот останется в реакционной колбе в виде дибромэтана, представляющего собой жидкость.
Особым образом стоит отметить реакцию алкенов в газовой фазе при сильном нагревании, например, с хлором.
При таких условиях протекает не реакция присоединения, а реакция замещения. При чем исключительно по альфа-атому углерода, то есть атому, соседствующему с двойной связью. В данном случае получается 3-хлорпропен-1. Эти реакции на экзамене встречаются нечасто, поэтому большинство учеников их не помнит и, как правило, совершает ошибки.
Четвертым номером идет реакция гидрирования, а вместе с ней и реакция дегидрирования. То есть присоединение или отщепление водорода.
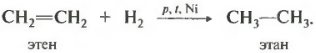
Гидрирование происходит при не очень высокой температуре на никелевом катализаторе. При более высокой температуре возможно дегидрирование с получением алкинов.
Пятым свойством алкенов является способность к полимеризации, когда сотни и тысячи молекул алкена за счет разрыва пи-связи и образования сигма-свзяей друг с другом образуют очень длинные и прочные цепочки.
В данном случае получился полиэтилен. Обратите внимание, что в получившейся молекуле кратные связи отсутствуют. Такие вещества называются полимерами, исходные молекулы называются мономерами, повторяющийся фрагмент это элементарное звено полимера, а число n степень полимеризации.
Также возможны реакции получения других важных полимерных материалов, например, полипропилена.
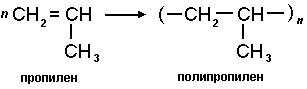
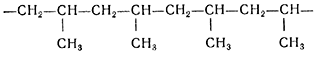
Еще один важный полимер поливинилхлорид.
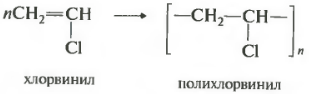
Исходным веществом для производства этого полимера является хлорэтен, тривиальное название которого винилхлорид. Поскольку этот непредельный заместитель называется винил. Часто встречающаяся аббревиатура на пластмассовых изделиях ПВХ как раз расшифровывается как поливинилхлорид.
Мы обсудили пять свойств, которые представляли собой реакции присоединения по двойной связи. Теперь обратимся к реакциям окисления .
Реакции окисления алкенов
Шестое химическое свойство в нашем общем списке это мягкое окисление или реакция Вагнера. Оно протекает при воздействии на алкен водным раствором перманганата калия на холоду, поэтому часто в экзаменационных заданиях указывают температуру ноль градусов.
В результате получается двухатомный спирт. В данном случае этиленгликоль, а в целом такие спирты носят общее название гликоли. В процессе реакции фиолетово-розовый раствор перманганата обесцвечивается, поэтому эта реакция также является качественной на двойную связь. Марганец в нейтральной среде из степени окисления +7 восстанавливается до степени окисления +4. Рассмотрим еще несколько примеров. УРАВНЕНИЕ
Здесь получился пропандиол-1,2. Однако таким же образом будут реагировать и циклические алкены. УРАВНЕНИЕ
Еще один вариант, когда двойная связь находится, например, в боковой цепи ароматических углеводородов. Регулярно в заданиях егэ встречается реакция Вагнера с участием стирола, его второе название винилбензол.
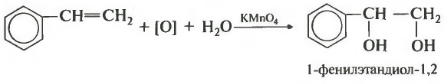
Я надеюсь, что представил вашему вниманию достаточно примеров, чтобы вы поняли, что мягкое окисление двойной связи всегда подчиняется довольно простому правилу пи-связь разрывается и к каждому атому углерода присоединяется гидроксигруппа.
Теперь, что касается жесткого окисления. Это будет наше седьмое свойство. Такое окисление происходит, когда алкен реагирует с кислотным раствором перманганата калия при нагревании.
Происходит деструкция молекулы, то есть ее разрушение по двойной связи. В случае бутена-2 получились две молекулы уксусной кислоты. В целом же, по продуктам окисления можно судить о положении кратной связи в углеродной цепи.
При окислении бутена-1 получается молекула пропионовой (пропановой) кислоты и углекислый газ.
В случае этилена получится две молекулы углекислого газа. Во всех случаях в кислой среде марганец из степени окисления +7 восстанавливается до +2.
И, наконец, восьмое свойство полное окисление или горение.
Алкены сгорают, как и другие углеводороды, до углекислого газа и воды. Запишем уравнение сгорания алкенов в общем виде.
Молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле алкена, поскольку в состав молекулы CO 2 входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть 2n/2, а значит просто n.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа плюс n из воды, итого 3n. Слева атомов кислорода столько же, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть 3n/2 молекул кислорода. Можно записать 1,5n.
Мы рассмотрели восемь химических свойств алкенов.
Алке́ны (олефины , этиленовые углеводороды C n H 2n
Гомологический ряд.
|
этен (этилен) | |
Простейшим алкеном является этилен (C 2 H 4). По номенклатуре IUPAC названия алкенов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ен»; положение двойной связи указывается арабской цифрой.
Углеводородные радикалы, образованные от алкенов имеют суффикс «-енил» . Тривиальные названия: CH 2 =CH- «винил» , CH 2 =CH-CH 2 - «аллил» .
Атомы углерода при двойной связи находятся в состоянии sp² гибридизации, и имеют валентный угол 120°.
Для алкенов характерны изомерия углеродного скелета, положения двойной связи, межклассовая и пространственная.
Физические свойства
Температуры плавления и кипения алкенов (упрощенно) увеличиваются с молекулярной массой и длиной главной углеродной цепи.
При нормальных условиях алкены с C 2 H 4 до C 4 H 8 - газы; с пентена C 5 H 10 до гексадецена C 17 H 34 включительно - жидкости, а начиная с октадецена C 18 H 36 - твёрдые вещества. Алкены не растворяются в воде, но хорошо растворяются в органических растворителях.
Дегидрирование алканов
Это один из промышленных способов получения алкенов
Гидрирование алкинов
Частичное гидрирование алкинов требует специальных условий и наличие катализатора
Двойная связь является сочетания сигма- и пи-связей. Сигма- связь возникает при осевом перекрывании sp2 – орбиталей, а пи-связь при боковом перекрывании
Правило Зайцева:
Отщепление атома водорода в реакциях элиминирования происходит преимущественно от наименее гидрогенизированного атома углерода.
13. Алкены. Строение. sp 2 гибридизация, параметры кратной связи. Реакции электрофильного присоединения галогенов, галогеноводородов, хлорноватистой кислоты. Гидратация алкенов. Правило Морковникова. Механизмы реакций.
Алке́ны (олефины , этиленовые углеводороды ) - ациклические непредельные углеводороды, содержащие одну двойную связьмежду атомами углерода, образующие гомологический ряд с общей формулой C n H 2n
Одна s- и 2 p-орбитали смешиваются и образуются 2 равноценные sp2-гибридные орбитали, расположенные в одной плоскости под углом 120.
Если связь образуется более чем одной парой электронов, то она называется кратной .
Кратная связь образуется в тех случаях, когда имеется слишком мало электронов и связывающихся атомов, чтобы каждая пригодная для образования связи валентная орбиталь центрального атома могла перекрыться с какой-либо орбиталью окружающего атома.
Реакции электрофильного присоединения
В данных реакциях атакующей частицей является электрофил.
Галогенирование:
Гидрогалогенирование
Электрофильное присоединение галогенводородов к алкенам происходит по правилу Марковникова
Марковникова правило
Присоединение хлорноватистой кислоты с образованием хлоргидринов:
Гидратация
Реакция присоединения воды к алкенам протекает в присутствии серной кислоты :
Карбкатион - частица, в которой на атоме углерода сосредоточен положительный заряд, атом углерода имеет вакантную p-орбиталь.
14. Этиленовые углеводороды. Химические свойства: реакции с окислителями. Каталитическое окисление, реакция с надкислотами, реакция окисления до гликолей, с разрывом связи углерод-углерод, озонирование. Вакер-процесс. Реакции замещения.
Алке́ны (олефины , этиленовые углеводороды ) - ациклические непредельные углеводороды, содержащие одну двойную связьмежду атомами углерода, образующие гомологический ряд с общей формулой C n H 2n
Окисление
Окисление алкенов может происходить в зависимости от условий и видов окислительных реагентов как с разрывом двойной связи, так и с сохранением углеродного скелета.
При сжигании на воздухе олефины дают углекислый газ и воду.
H 2 C=CH 2 + 3O 2 => 2CO 2 + 2H 2 O
C n H 2n + 3n/O 2 => nCO 2 + nH 2 O – общая формула
Каталитическое окисление
В присутствии солей палладия этилен окисляется до ацетальдегида. Аналогично образуется ацетон из пропена.
При действии на алкены сильных окислителей (KMnO 4 или K 2 Cr 2 O 7 в среде Н 2 SO 4) при нагревании происходит разрыв двойной связи:
При окислении алкенов разбавленным раствором марганцовки образуются двухатомные спирты – гликоли (реакция Е.Е.Вагнера). Реакция протекает на холоде.
Ациклические и циклические алкены при взаимодействии с надкислотами RCOOOH в неполярной, среде образуют эпоксиды (оксираны), поэтому сама реакция носит название реакции эпоксидирования.

Озонирование алкенов.
при взаимодействии алкенов с озоном образуются перекисные соединения, которые называются озо-нидами. Реакция алкенов с озоном является наиболее важным методом окислительного расщепления алкенов по двойной связи
Алкены не вступают в реакции замещения.
Вакер-процесс -процесс получения ацетальдегида прямым окислением этилена.
Вакер-процесс основан на реакции окисления этилена дихлоридом палладия:
CH 2 =CH 2 + PdCl 2 + H 2 O = CH 3 CHO + Pd + 2HCl
15. Алкены: химические свойства. Гидрирование. Правило Лебедева. Изомеризация и олигомеризация алкенов. Радикальная и ионная полимеризация. Понятие полимер, олигомер, мономер, элементарное звено, степень полимеризации. Теломеризация и сополимеризация.
Гидрирование
Гидрирование алкенов непосредственно водородом происходит только в присутствии катализатора. Катализаторами гидрирования служат платина,палладий, никель
Гидрирование можно проводить и в жидкой фазе с гомогенными катализаторами
Реакции изомеризации
При нагревании возможна изомеризация молекул алкенов, которая
может привести как к перемещению двойной связи, так и к изменению скелета
углеводорода.
CH2=CH-CH2-CH3 CH3-CH=CH-CH3
Реакции полимеризации
Это разновидность реакции присоединения. Полимеризация - это реакция последовательного соединения одинаковых молекул в большие по размеру молекулы, без выделения какого-либо низкомолекулярного продукта. При полимеризации атом водорода присоединяется к наиболее гидрогенизированному атому углерода, находящемуся у двойной связи, а к другому атому углерода присоединяется остальная часть молекулы.
CH2=CH2 + CH2=CH2 + ... -CH2-CH2-CH2-CH2- ...
или n CH2=CH2 (-CH2-CH2-)n (полиэтилен)
Вещество, молекулы которого вступают в реакцию полимеризации, называются мономером . Молекула мономера обязательно должна иметь хотя бы одну двойную связь. Образующиеся полимеры состоят из большого количества повторяющихся цепочек, имеющих одинаковое строение (элементарных звеньев). Число, показывающее, сколько раз в полимере повторяется структурное (элементарное) звено, называется степенью полимеризации (n).
В зависимости от вида промежуточных частиц, образующихся при полимеризации, различают 3 механизма полимеризации: а) радикальный; б)катионный; в) анионный.
По первому методу получают полиэтилен высокого давления:
Катализатором реакции выступают пероксиды.
Второй и третий методы предполагает использование в качестве катализаторов кислот (катионная полимеризация), металлорганических соединений.
В химии олигомер ) - молекула в виде цепочки изнебольшого числа одинаковых составных звеньев.
Теломеризация
Теломеризация – олигомеризация алкенов в присутствии веществ – передатчиков цепи (телогенов). В результате реакции образуется смесь олигомеров (теломеров), концевые группы которых представляют собой части телогена. Например, в реакции CCl 4 с этиленом телогеном является CCl 4 .
CCl 4 + nCH 2 =CH 2 => Cl(CH 2 CH 2) n CCl 3
Инициирование этих реакций может осуществляться радикальными инициаторами или g -излучением.
16. Алкены. Реакции радикального присоединения галогенов и галогеноводородов (механизм). Присоединение карбенов к олефинам. Этилен, пропилен, бутилены. Промышленные источники и основные пути использования.
Алкены легко присоединяют галогены, особенно хлор и бром (галогенирование).
Типичной реакцией такого типа является обесцвечивание бромной воды
CH2=CH2 + Вr2 → СH2Br-CH2Br (1,2-дибромэтан)
Электрофильное присоединение галогенводородов к алкенам происходит по правилу Марковникова:
Марковникова правило : при присоединении протонных кислот или воды к несимметричным алкенам или алкинаматом водорода присоединяется к наиболее гидрогенизированному атому углерода
гидрогенизированный атом углерода – тот атом, к которому присоединен водород. Наиболее гидрогенизированный – там где больше всего Н
Реакции присоединения карбенов
Карбены CR 2: - высокореакционные короткоживущие частицы, которые способны легко присоединяться к двойной связи алкенов . В результате реакции присоединения карбена образуются производные циклопропана
Этиле́н - органическое химическое описываемое формулой С 2 H 4 . Является простейшималкеном (олефином )соединение. При нормальных условиях - бесцветный горючий газ со слабым запахом. Частично растворим в воде. Содержит двойную связь и поэтому относится к ненасыщенным или непредельным углеводородам. Играет чрезвычайно важную роль в промышленности. Этилен - самое производимое органическое соединение в мире: Окись этилена; полиэтилен, уксусная кислота, этиловый спирт.
Основные химические свойства (не учи, просто пусть будут на всякий случай, вдруг списать получится)
Этилен - химически активное вещество. Так как в молекуле между атомами углерода имеется двойная связь, то одна из них, менее прочная, легко разрывается, и по месту разрыва связи происходит присоединение, окисление, полимеризация молекул.
Галогенирование:
CH 2 =CH 2 + Br 2 → CH 2 Br-CH 2 Br
Происходит обесцвечивание бромной воды. Это качественная реакция на непредельные соединения.
Гидрирование:
CH 2 =CH 2 + H - H → CH 3 - CH 3 (под действием Ni)
Гидрогалогенирование:
CH 2 =CH 2 + HBr → CH 3 - CH 2 Br
Гидратация:
CH 2 =CH 2 + HOH → CH 3 CH 2 OH (под действием катализатора)
Эту реакцию открыл A.M. Бутлеров, и она используется для промышленного получения этилового спирта.
Окисление:
Этилен легко окисляется. Если этилен пропускать через раствор перманганата калия, то он обесцветится. Эта реакция используется для отличия предельных и непредельных соединений. Окись этилена - непрочное вещество, кислородный мостик разрывается и присоединяется вода, в результате образуетсяэтиленгликоль. Уравнение реакции :
3CH 2 =CH 2 + 2KMnO 4 + 4H 2 O → 3HOH 2 C - CH 2 OH + 2MnO 2 + 2KOH
C 2 H 4 + 3O 2 → 2CO 2 + 2H 2 O
Полимеризация (получение полиэтилена):
nCH 2 =CH 2 → (-CH 2 -CH 2 -) n
Пропиле́н (пропен) СН 2 =СН-СН 3 - непредельный (ненасыщенный) углеводород ряда этилена, горючий газ. Пропилен представляет собой газообразное вещество с низкой температурой кипения t кип = −47,6 °C
Обычно пропилен выделяют из газов нефтепереработки (при крекинге сырой нефти, пиролизе бензиновых фракций) или попутных газов, а также из газов коксования угля.
Тема урока: Алкены. Получение, химические свойства и применение алкенов.
Цели и задачи урока:
- рассмотреть конкретные химические свойства этилена и общие свойства алкенов;
- углубить и конкретизировать понятия о?-связи, о механизмах химических реакций;
- дать первоначальные представления о реакциях полимеризации и строении полимеров;
- разобрать лабораторные и общие промышленные способы получения алкенов;
- продолжить формирование умения работать с учебником.
Оборудование: прибор для получения газов, раствор КМnO 4 , этиловый спирт, концентрированная серная кислота, спички, спиртовка, песок, таблицы «Строение молекулы этилена», «Основные химические свойства алкенов», демонстрационные образцы «Полимеры».
ХОД УРОКА
I. Организационный момент
Мы продолжаем изучение гомологического ряда алкенов. Сегодня нам предстоит рассмотреть способы получения, химические свойства и применение алкенов. Мы должны охарактеризовать химические свойства, обусловленные двойной связью, получить первоначальные представления о реакциях полимеризации, рассмотреть лабораторные и промышленные способы получения алкенов.
II. Активизация знаний учащихся
- Какие углеводороды называются алкенами?
- Каковы особенности их строения?
- В каком гибридном состоянии находятся атомы углерода, образующие двойную связь в молекуле алкена?
Итог: алкены отличаются от алканов наличием в молекулах одной двойной связи, которая обуславливает особенности химических свойств алкенов, способов их получения и применения.
III. Изучение нового материала
1. Способы получения алкенов
Составить уравнения реакций, подтверждающих способы получения алкенов
– крекинг алканов C 8 H 18 ––> C
4 H
8
+ C 4 H 10 ; (термический крекинг при 400-700 o С)
октан
бутен
бутан
– дегидрирование алканов C 4 H 10 ––> C 4 H 8
+ H 2 ; (t, Ni)
бутан
бутен
водород
– дегидрогалогенирование галогеналканов C 4 H 9 Cl
+ KOH ––> C 4 H 8 + KCl
+ H 2 O;
хлорбутан
гидроксид бутен
хлорид
вода
калия
калия
– дегидрогалогенирование дигалогеналканов 
– дегидратация спиртов С 2 Н 5 ОН ––> С 2 Н 4
+ Н 2 О (при нагревании в присутствии
концентрированной серной кислоты)
Запомните!
При реакиях
дегидрирования, дегидратации,
дегидрогалогенирования и дегалогенирования
нужно помнить, что водород преимущественно
отрывается от менее гидрогенизированных атомов
углерода (правило Зайцева, 1875 г.)
2. Химические свойства алкенов
Характер углерод – углеродной связи
определяет тип химических реакций, в которые
вступают органические вещества. Наличие в
молекулах этиленовых углеводородов двойной
углерод – углеродной связи обуславливает
следующие особенности этих соединений:
– наличие двойной связи позволяет отнести
алкены к ненасыщенным соединениям. Превращение
их в насыщенные возможно только в результате
реакций присоединения, что является основной
чертой химического поведения олефинов;
– двойная связь представляет собой значительную
концентрацию электронной плотности, поэтому
реакции присоединения носят электрофильный
характер;
– двойная связь состоит из одной - и одной -связи, которая достаточно легко
поляризуется.
Уравнения реакций, характеризующих химические свойства алкенов
а) Реакции присоединения
Запомните! Реакции замещения свойственны алканам и высшим циклоалканам, имеющим только одинарные связи, реакции присоединения – алкенам, диенам и алкинам, имеющим двойные и тройные связи.

Запомни! Возможны следующие механизмы разрыва -связи:
а) если алкены и реагент – неполярные соединения, то -связь разрывается с образованием свободного радикала:
H 2 C = CH 2 + H: H ––> + +
б) если алкен и реагент – полярные соединения, то разрыв -связи приводит к образование ионов:
в) при соединении по месту разрыва -связи реагентов, содержащих в составе молекулы атомы водорода, водород всегда присоединяется к более гидрированному атому углерода (правило Морковникова, 1869 г.).
– реакция полимеризации nCH 2 = CH 2
––> n – CH 2 – CH 2 –– > (– CH 2 – CH 2
–)n
этен
полиэтилен
б) реакция окисления
Лабораторный опыт. Получить этилен и изучить его свойства (инструкция на столах учащихся)
Инструкция по получению этилена и опытов с ним
1. Поместите в пробирку 2 мл концентрированной
серной кислоты, 1 мл спирта и небольшое
количество песка.
2. Закройте пробирку пробкой с газоотводной
трубкой и нагрейте в пламени спиртовки.
3. Выделяющийся газ пропустите через раствор с
перманганатом калия. Обратите внимание на
изменение цвета раствора.
4. Подожгите газ у конца газоотводной трубки.
Обратите внимание на цвет пламени.
– алкены горят светящимся пламенем. (Почему?)
C 2 H 4 + 3O 2 ––> 2CO 2 + 2H 2 O (при полном окислении продуктами реакции являются углекислый газ и вода)
Качественная реакция: «мягкое окисление (в водном растворе)»
– алкены обесцвечивают раствор перманганата калия (реакция Вагнера)
При более жёстких условиях в кислой среде продуктами реакции могут быть карбоновые кислоты, например (в присутствии кислот):
CH 3 – CH = CH 2 + 4 [O] ––> CH 3 COOH + HCOOH
– каталичесикое окисление
Запомните главное!
1. Непредельные углеводороды активно вступают в
реакции присоединения.
2. Реакционная активность алкенов связана с тем,
что - связь под
действием реагентов легко разрывается.
3. В результате присоединения происходит переход
атомов углерода из sp 2 – в sp 3 -
гибридное состояние. Продукт реакции имеет
предельный характер.
4. При нагревании этилена, пропилена и других
алкенов под давление или в присутствии
катализатора их отдельные молекулы соединяются
в длинные цепочки – полимеры. Полимеры
(полиэтилен, полипропилен) имеют большое
практическое значение.
3. Применение алкенов (сообщение учащегося по следующему плану).
1 – получение горючего с высоким октановым числом;
2 – пластмасс;
3 – взрывчатых веществ;
4 – антифризов;
5 – растворителей;
6 – для ускорения созревания плодов;
7 – получение ацетальдегида;
8 – синтетического каучука.
III. Закрепление изученного материала

Домашнее задание: §§ 15, 16, упр. 1, 2, 3 стр. 90, упр. 4, 5 стр. 95.





