Строение карбоксильной группы и карбоксилат-аниона. Карбоновые кислоты
Карбоновыми кислотами называют соединения, в которых содержится карбоксильная группа:
Карбоновые кислоты различают:
- одноосновные карбоновые кислоты;
- двухосновные (дикарбоновые) кислоты (2 группы СООН ).
В зависимости от строения карбоновые кислоты различают:
- алифатические;
- алициклические;
- ароматические.
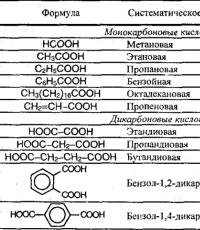
Примеры карбоновых кислот.


Получение карбоновых кислот.
1. Окисление первичных спиртов перманганатом калия и дихроматом калия:

2. Гибролиз галогензамещенных углеводородов, содержащих 3 атома галогена у одного атома углерода:
3. Получение карбоновых кислот из цианидов:
При нагревании нитрил гидролизуется с образованием ацетата аммония:
При подкисления которого выпадает кислота:
4. Использование реактивов Гриньяра:
5. Гидролиз сложных эфиров:
6. Гидролиз ангидридов кислот:
7. Специфические способы получения карбоновых кислот:
Муравьиная кислота получается при нагревании оксида углерода (II) с порошкообразным гидроксидом натрия под давлением:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
Бензойную кислоту получают окислением монозамещенных гомологов раствором перманганата калия:
Реакция Каннициаро . Бензальдегид обрабатывают 40-60% раствором гидроксида натрия при комнатной температуре.

Химические свойства карбоновых кислот.
В водном растворе карбоновые кислоты диссоциируют:

Равновесие сдвинуто сильно влево, т.к. карбоновые кислоты являются слабыми.
Заместители влияют на кислотность вследствие индуктивного эффекта. Такие заместители оттягивают электронную плотность на себя и на них возникает отрицательный индуктивный эффект (-I). Оттягивание электронной плотности приводит к повышению кислотности кислоты. Электронодонорные заместители создают положительный индуктивный заряд.

1. Образование солей. Реагирование с основными оксидами, солями слабых кислот и активными металлами:

Карбоновые кислоты - слабые, т.к. минеральные кислоты вытесняют их из соответствующих солей:
2. Образование функциональных производных карбоновых кислот:
3. Сложные эфиры при нагревании кислоты со спиртом в присутствие серной кислоты - реакция этерификации:
4. Образование амидов, нитрилов:
3. Свойства кислот обуславливаются наличием углеводородного радикала. Если протекает реакция в присутствие красного фосфора, то образует следующий продукт:
4. Реакция присоединения.

8. Декарбоксилирование. Реакцию проводят сплавлением щелочи с солью щелочного металла карбоновой кислоты:
9. Двухосновная кислота легко отщепляет СО 2
при нагревании:
Дополнительные материалы по теме: Карбоновые кислоты.
Калькуляторы по химии |
|
| Химия онлайн на нашем сайте для решения задач и уравнений. | |
[ее рисунок, (гидр43)]
Карбоксильная группа представляет собой плоскую сопряженную систему, в которой возникает р,-сопряжение при взаимодействии р z -орбитали атома кислорода гидроксогруппы с -связью. Наличие р,-сопряжения в карбоксильной группе карбоновых кислот способствует равномерному распределению отрицательного заряда в ацилат-ионе, образующемся при отщеплении протона.
[ацилат-ион, (гидр44)]
Равномерное распределение отрицательного заряда в ацилат-ионе показывают следующим образом: (гидр45)
Наличие р,-сопряжения в карбоксильной группе карбоновых кислот значительно повышает кислотные свойства карбоновых кислот по сравнению со спиртами.
С 2 Н 5 ОН рК а =18
СН 3 СООН рК а =4,76
В кабоновых кислотах частичный положительный заряд на карбонильном атоме углерода меньше, чем в альдегидах и кетонах, поэтому кислота менее активна к восприятию атаки нуклеофильного реагента. Соответственно, реакции нуклеофильного присоединения более характерны для альдегидов и кетонов.
R-гидрофобная часть молекулы;
СООН-гидрофильная часть молекулы.
С увеличением длины углеводородного радикала понижается растворимость кислот, степень гидратированности и стабильность ацилат-аниона. Это приводит к уменьшению силы карбоновых кислот.
В карбоновых кислотах выделяют следующие реакционные центры: (гидр46)
1. основный нуклеофильный центр;
2. электрофильный центр;
3. ОН-кислотный центр;
4. СН-кислотный центр;
Химические свойства карбоновых кислот
I. Реакции диссоциации.
[карб. к-та+вода= ацилат-ион+ H 3 O + , (гидр47)]
II. Реакции галогенирования (реакции в СН-кислотном центре)
[пропионовая к-та+ Br 2 =α-бромпропионовая +HBr, (гидр48)]
III. Реакции декарбоксилирования - реакции, в ходе которых происходит удаление углекислого газа из карбоксильной группы, приводящее к разрушению карбоксильной группы.
In vitro pеакции декарбоксилирования протекают при нагревании; in vivo – с участием ферментов-декарбоксилаз.
1. [пропановая к-та= угл. газ+ этан, (гидр49)]
2. В организме декарбоксилирование дикарбоновых кислот протекает ступенчато: [янтарная= пропионовая + угл. газ=этан+ угл. газ, (гидр50)]
3. В организме также протекает окислительное декарбоксилирование, в частности, ПВК в митохондриях. С участием декарбоксилазы, дегидрогеназы и кофермента А (HS-KoA). [ПВК= этаналь+ угл. газ= ацетил-Ко-А+ НАДН+ Н + , (гидр51)]
Ацетил-КоА, будучи активным соединением, вовлекается в цикл Кребса.
IV. Реакции этерификации – нуклеофильного замещения (S N) у sр 2 -гибридизованного атома углерода. [уксусная к-та+ метанол= метилацетат, (гидр52)]
Механизм реакции нуклеофильного замещения, (гидр53)
V. Реакции окисления.
Рассмотрим на примере гидроксокислот. Окисление гидроксокислот протекает аналогично окислению вторичных спиртов с участием ферментов-дегидрогеназ.
1. [молочная= ПВК +НАДН+ Н + , (гидр54)]
2. [β-гидроксимасляная= ацетоуксусная +НАДН+ Н + , (гидр55)]
Т.о., при окислении гидроксокислот с участием ферментов-дегидрогеназ образуются кетокислоты.
Пути превращения ацетоуксусной кислоты в организме:
В норме она подвергается гидролитическому расщеплению с участием фермента гидролазы, при этом образуются 2 молекулы уксусной кислоты: [ацетоуксусная+ вода=2 уксусной к-ты, (гидр56)]
При патологии ацетоуксусная кислота декарбоксилируется с образованием ацетона: [ацетоуксусная к-та=ацетон+ угл. газ, (гидр57)]
Кетоновые тела накапливаются в крови больных сахарным, обнаруживаются в моче, они токсичны, особенно для нервной системы.
Карбоновые кислоты – органические соединения, содержащие одну или несколько карбоксильных групп –СООН. Название происходит от лат. carbo – уголь и греч. oxys – кислый.
Карбоксильная группа (сокращенно -COOH) - функциональная группа карбоновых кислот - состоит из карбонильной группы и связанной с ней гидроксильной группы.
В молекулах карбоновых кислот p-электроны атомов кислорода гидроксильной группы взаимодействуют с электронами p -связи карбонильной группы, в результате чего возрастает полярность связи O-H, упрочняется p -связь в карбонильной группе, уменьшается частичный заряд (d +) на атоме углерода и увеличивается частичный заряд (d +) на атоме водорода.
В результате связь О–Н становится настолько поляризованной, что водород способен «отрываться» в виде протона. Происходит процесс кислотной диссоциации:
2. Классификация карбоновых кислот. Карбоновые кислоты: насыщенные, ненасыщенные, ароматические; одноосновные, двухосновные, замещенные.
По основности (т.е. числу карбоксильных групп в молекуле) карбоновые кислоты можно разделить на несколько групп:
Одноосновные (монокарбоновые, одна группа - СООН) RCOOH;
например, CH 3 CH 2 CH 2 COOH;
HOOC-CH 2 -COOH пропандиовая (малоновая) кислота, щавелевая кислота HOOC-COOH;
Бензол – 1,4 – дикарбоновая (терефталевая) кислота;
Трехосновные (трикарбоновые) R(СООН) 3 кислоты и т.д.
По строению углеводородного радикала, с которым связана карбоксильная группа, карбоновые кислоты подразделяются на:
Алифатические карбоновые кислоты:
а) насыщенные, или предельные, например, уксусная CH 3 COOH кислота;
б) ненасыщенные, или непредельные, например, CH 2 =CHCOOH пропеновая (акри-
ловая) кислота;
Алициклические, например, циклогексанкарбоновая кислота;
Ароматические, например, бензойная кислота;
Бензол – 1,2 – дикарбоновая (фталевая) кислота.
Если в углеводородном радикале карбоновых кислот атом (атомы) водорода замещен на другие функциональные группы, то такие кислоты называются гетерофункциональными. Среди них различают:
Галогенкарбоновые (например, CH 2 Cl-COOH хлоруксусная кислота);
Нитрокислоты (например, NO 2 -С 6 Н 4 СООН нитробензойная кислота);
Аминокислоты (например, NH 2 -СН 2 СООН аминоуксусная кислота);
Оксикислоты (например, молочная СН 3 -СН-СООН) и др.
Насыщенные одноосновные карбоновые кислоты. Муравьиная и уксусная кислоты как представители насыщенных одноосновных карбоновых кислот, их состав, строение, молекулярные, структурные и электронные формулы.
Формула гомологического ряда кислот С n Н 2n О 2 (n≥1) или С n Н 2n+1 CООН (n≥0). По числу углеродных атомов карбоновые кислоты классифицируют на обычные (С 1 -С 10) и высшие (>С 10) кислоты. Карбоновые кислоты с числом атомов углерода выше 6 называют высшими (жирными) кислотами. Название "жирные" эти кислоты получили потому, что большинство из них могут быть выделены из жиров.
Простейшим представителем насыщенных одноосновных карбоновых кислот является муравьиная кислота: СН 2 О 2 (молекулярная формула), Н-СООН, (структурные формулы),
(электронная формула).
Следующим представителем гомологического ряда насыщенных одноосновных карбоновых кислот является уксусная кислота: С 2 Н 4 О 2 (молекулярная формула), СН 3 СООН, (структурные формулы),
(электронная формула).
Карбоксильная группа (карбоксил ) -СООН - функциональная одновалентная группа, входящая в состав карбоновых кислот и определяющая их кислотные свойства.
Строение карбоксильной группы
Карбоксильная группа сочетает в себе две функциональные группы - карбонил (>C=O) и гидроксил (-OH), взаимно влияющие друг на друга.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О-Н.
В водном растворе карбоновые кислоты диссоциируют на ионы:
R-COOH = R-COO − + H +
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей .
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
| Бензол | Это заготовка статьи по органической химии . Вы можете помочь проекту, дополнив её. |
Напишите отзыв о статье "Карбоксильная группа"
Отрывок, характеризующий Карбоксильная группа
– Светодар, Север... Что стало с ним? Как прожил свою жизнь на Земле сын Радомира и Магдалины?..Север задумался... Наконец, глубоко вздохнув, будто сбрасывая наваждение прошлого, начал свой очередной захватывающий рассказ...
– После распятия и смерти Радомира, Светодара увезли в Испанию рыцари Храма, чтобы спасти его от кровавых лап «святейшей» церкви, которая, чего бы это ни стоило, пыталась найти и уничтожить его, так как мальчик являлся самым опасным живым свидетелем, а также, прямым продолжателем радомирова Дерева Жизни, которое должно было когда-нибудь изменить наш мир.
Светодар жил и познавал окружающее в семье испанского вельможи, являвшегося верным последователем учения Радомира и Магдалины. Своих детей, к их великой печали, у них не было, поэтому «новая семья» приняла мальчика очень сердечно, стараясь создать ему как можно более уютную и тёплую домашнюю обстановку. Назвали его там Амори (что означало – милый, любимый), так как своим настоящим именем называться Святодару было опасно. Оно звучало слишком необычно для чужого слуха, и рисковать из-за этого жизнью Светодара было более чем неразумно. Так Светодар для всех остальных стал мальчиком Амори, а его настоящим именем звали его лишь друзья и его семья. И то, лишь тогда, когда рядом не было чужих людей...
КАРБОКСИЛ, КАРБОКСИЛЬНАЯ группа [карбо… + гр. кислый] – одноатомная группа COOH, характеризующая органические, т. наз. карбоновые кислоты, например, уксусная кислота CH3COOH Большой словарь иностранных слов. Издательство «ИДДК», 2007 … Словарь иностранных слов русского языка
КАРБОКСИЛЬНАЯ ГРУППА - (карбоксил), СООН кислотная группа С, присутствующая в (см.); число К. г. определяет основность кислоты … Большая политехническая энциклопедия
Карбоксигруппа, карбоксил, одновалентная группа характерная для карбоновых кислот. Состоит из карбонильной и гидроксильной (ОН) групп (отсюда назв.: карб + оксил) … Большой энциклопедический политехнический словарь
Карбоксил, функциональная одновалентная группировка Карбоновые кислоты) и определяющая их кислотные свойства … Большая советская энциклопедия
карбоксильная группа - карбоксил … Cловарь химических синонимов I
A одновалентная гр. СООН, присутствие которой определяет принадлежность орг. соединения к карбоновым кислотам. Пример: уксусная кислота СНзСООН. При замещении в К. водорода металлом образуются соли, при замещении водородастиртовым радикалом… … Геологическая энциклопедия
Бензил ацетат имеет эфирную функциональную группу (показанно красным), ацетильную группу (зелёная) и бензильную группу (оранжевая). Функциональная группа структурный фрагмент органическо … Википедия
функциональная группа - Functional Group Функциональная группа Cтруктурный фрагмент молекулы, характерный для данного класса органических соединений и определяющий его химические свойства. Примеры функциональных групп: азидная, гидроксильная, карбонильная,… … Толковый англо-русский словарь по нанотехнологии. - М.